Zu den Möglichkeiten und Gefahren der nichtinvasiven Pränataldiagnostik - vor allem mit Blick auf die Trisomie 21 - gibt es unterschiedliche Ansichten. Im Beitrag von Klaus Zerres geht es um die Pro-Position. Den Beitrag zur Contra-Position finden Sie hier.
In Irland war vor dem Referendum zur gesetzlichen Neuregelung der Schwangerschaftsabbrüche am 25.05.2018 auf großen Plakatwänden zu lesen: "100.000 Menschen leben heute wegen unserer Gesetze zum Schwangerschaftsabbruch. Warum das ändern?".
Die Iren stimmten mit großer Mehrheit für die Änderung des Gesetzes, womit auch dort in Zukunft Schwangerschaftsabbrüche unter bestimmten Bedingungen legal sein werden. "Pro Choice"-Verfechter feiern diese Entscheidung als Errungenschaft autonomer Reproduktion,
"Pro Life"-Verfechter sehen dadurch fundamentale moralische Werte verletzt. Die Legitimität von Schwangerschaftsabbrüchen nach pränataler Diagnostik (PD) fetaler Auffälligkeiten wird auch in der Bundesrepublik kontrovers diskutiert.
Der Schwerpunkt der nachfolgenden Betrachtungen soll auf Aspekten der Anwendung pränataler nichtinvasiver Tests (NIPT) zur vorgeburtlichen Erkennung des Down-Syndroms (DS) bzw. der Trisomie 21 liegen, auf die sich die öffentliche Diskussion fokussiert, obwohl heute unterschiedliche NIPTs verfügbar sind, die neben dem DS weitere Trisomien, Geschlechtschromosomen-Störungen, verschiedene Mikrodeletionssyndrome und einzelne monogene Krankheiten erfassen. Sie bedürfen sowohl hinsichtlich der Aussagekraft wie ihrer ethischen Einordnung jeweils einer unterschiedlichen Betrachtung, die den Rahmen dieser kurzen Ausführungen sprengen würde.
Die Sorge einer zunehmenden Inanspruchnahme von NIPTs, die durch die Übernahme der Kosten durch die GKV beschleunigt und damit gewissermaßen legitimiert werden könnte, besteht darin, dass sich zukünftige Eltern unter Druck gesetzt fühlen können, diese Verfahren auch in Anspruch zu nehmen ("Routinisierung") [1]. Es wird weiterhin befürchtet, dass sich durch eine geringere Anzahl von Menschen mit DS in unserer Gesellschaft deren Lebenssituation verschlechtern könnte, obwohl sich diese seit Jahrzehnten trotz existierender Möglichkeiten der PD kontinuierlich verbessert hat. Obwohl für beide Befürchtungen bisher keine systematischen wissenschaftlichen Belege existieren, müssen sie dennoch ernst genommen werden.
Weniger Geburten bei steigendem mütterlichen Alter führen bei Überschätzung kindlicher Risiken zu vermehrter Nachfrage nach PD
Die Zahl der Geburten sinkt in westlichen Industriegesellschaften bei steigendem mütterlichen Alter. Die einzelne Schwangerschaft rückt damit immer mehr in den Lebensmittelpunkt.
Die Wahrscheinlichkeit für die Geburt eines Kindes mit DS beträgt für eine 40-jährige Frau statistisch etwa 1 %. In einer repräsentativen Befragung im Aachener Raum gaben bei 9 Antwortmöglichkeiten nur 10 % die richtige Antwort an, 46 % nannten Wahrscheinlichkeiten von mehr als 10 %, 14 % sogar von mehr als 30 % [2]. Aachener Studierende der Medizin gaben eher noch höhere Wahrscheinlichkeiten an.
In einer Studie der Bundeszentrale für gesundheitliche Aufklärung (BZgA) zu "Ansichten zur Pränataldiagnostik" haben 82 % der Befragten folgende Feststellung bejaht ("trifft voll und ganz zu"): "Führt zur Entlastung, weil es die Sorge vor einer Erkrankung des Kindes nehmen kann" und 76 % die Feststellung "Macht Frauen die Schwangerschaft sicherer" [3]. Diese Einstellung erklärt die große Nachfrage nach PD, auf die das Angebot von IGeL-Leistungen wie das Ersttrimester-Screening schon seit Jahren reagiert. NIPTs werden, wie die weltweite Entwicklung zeigt, von einer wachsenden Anzahl von Schwangeren in Anspruch genommen.
Rasante Weiterentwicklung der nichtinvasiven PD
Ein wissenschaftliches Ziel mehrerer Forschergenerationen war und ist es, die Wahrscheinlichkeit einer Schwangeren für die Geburt eines Kindes mit einer Chromosomenstörung möglichst präzise zu ermitteln. Das mütterliche Alter war lange alleiniger Parameter und dies führte dazu, dass Schwangere, die 35 Jahre und älter sind, bis heute eine invasive Diagnostik mit kindlicher Chromosomenanalyse als GKV-Leistung in Anspruch nehmen können, womit ca. 50 % der Schwangerschaften mit Kindern mit DS erkannt werden könnten. Begründet wurde diese Altersgrenze vor allem mit dem bei invasiven Untersuchungen (Fruchtwasseruntersuchung ab der 16. Schwangerschaftswoche (SSW) oder Chorionzottenbiopsie ab der 11. SSW) bestehenden eingriffsbedingtem Risiko für eine Fehlgeburt von 0,5 % bis 1 %.
Seit den 80er-Jahren wird das Ersttrimester-Screening in verschiedenen Ausführungen zur genaueren Bestimmung der Wahrscheinlichkeit für kindliche Trisomien angeboten. Auf der Basis des "Altersrisikos" wird eine "Risiko-Adjustierung" in der 11. – 13. SSW vorgenommen, die eine Ultraschall-Bestimmung der Nackentransparenz sowie mütterliche Blutwerte (meist freies ß-hCG und PAPP-A) einbezieht. Ergibt sich eine erhöhte "adjustierte" Wahrscheinlichkeit für eine kindliche Trisomie (Grenzwert meist 1:300 bis 1:150), wird eine invasive Diagnostik angeboten. Durch NIPTs besteht seit 2011 die Möglichkeit, fetale DNA-Fragmente im mütterlichen Blut durch eine Hochdurchsatz-Sequenzierung molekulargenetisch zu analysieren und quantitativ zu bestimmen.
Was leisten nichtinvasive Pränataltests im Vergleich zu Amniozentese/Chorionzottenbiopsie und dem Ersttrimester-Screening?
Ersttrimester-Screening und nichtinvasive Pränataltests sind im Vergleich zu invasiven Diagnoseverfahren Screeninguntersuchungen. Auffällige Testergebnisse erfordern eine diagnostische invasive Untersuchung zur Bestätigung eines Verdachtes.
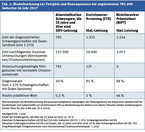
Im gegenteiligen Fall, also bei positivem ("ungünstigen") Ergebnis des NIPT ist die Wahrscheinlichkeit für ein kindliches DS sehr hoch. Sie kann durch den positiv prädiktiven Wert (PPW) ausgedrückt werden. Er besagt, in welchem Anteil der Fälle ein "ungünstiges" (positives) Testergebnis beim Kind tatsächlich vorliegt und durch eine invasive Untersuchung bestätigt wird. Die Höhe des PPW hängt von der Häufigkeit der Chromosomenstörung selbst und damit im Falle des DS vom Alter der Mutter ab. Er beträgt ca. 35 % für eine 20-jährige Schwangere (altersabhängige Wahrscheinlichkeit für die Geburt eines Kindes mit DS ca. 1:2.000) und steigt auf mehr als 90 % bei der 40-jährigen Schwangeren (altersabhängige Wahrscheinlichkeit für die Geburt eines Kindes mit DS ca. 1:100). Über alle Altersgruppen wird ein PPW von 0,66 angenommen (Tab. 1).
Die Testqualität des Ersttrimester-Screenings ist hinsichtlich der Aussagekraft im Vergleich zum NIPT wesentlich schlechter. Der PPW beträgt für das DS ca. 5 %, d. h., dass sich lediglich in einem von 20 Fällen mit auffälligem Ersttrimester-Screening-Testergebnis die Diagnose DS durch eine invasive Testung bestätigen lässt.
Modellrechnung
In Tabelle 1 sollen die möglichen Konsequenzen unterschiedlicher Strategien für die Erkennung des DS in einer stark vereinfachten Modellrechnung auf der Basis von 785.000 Geburten des Jahres 2017 verdeutlicht werden. Sie basiert auf der theoretischen vereinfachten Annahme, dass alle Frauen die jeweilige Diagnostik auch in Anspruch nehmen:- Spalte 1: alle Frauen, die 35 Jahre und älter sind (157.000) eine Amniozentese bzw. Chorionzottenbiopsie;
- Spalte 2: alle Schwangeren (785.000) das Ersttrimester-Screening bzw. in
- Spalte: 3 alle Schwangeren (785.000) einen NIPT.
Die Modellrechnung bezieht sich vereinfacht nur auf das DS.
In einem Anteil von 0,5 bis 4 % liefert NIPT keine verwertbare Aussage, die eine weitere Abklärung erfordert. Mögliche Optionen sind die Wiederholung des Tests, eine ultraschallbasierte Aussage bzw. zuletzt eine invasive Abklärung. Um das konkrete Ausmaß möglicher Konsequenzen abschätzen zu können, sind weitere Daten notwendig.
Inanspruchnahme vorgeburtlicher Screening- und Diagnoseverfahren
Verlässliche Zahlen zur Inanspruchnahme des Ersttrimester-Screenings als IGeL-Leistung sind nicht verfügbar. Invasive PD (Amniozentese und Chorionzottenbiopsie) ist auch wegen der zunehmenden Inanspruchnahme des Ersttrimester-Screenings seit Jahren stark rückläufig. 1997 wurden durch alle Leistungserbringer (bei 812.103 Geburten) 68.267 Amniozentesen/Chorionzottenbiopsien erbracht, wodurch allein eingriffsbedingt mehr als 4.000 Fehlgeburten(!) meist bei Schwangerschaften ohne Chromosomenveränderungen ausgelöst worden sein müssen.
Abbruchraten nach "ungünstigem" (positivem) NIPT-Ergebnis sinken. Abbrüche erfolgen früher als nach bisheriger PD
Internationale Daten, z. B. aus den USA und England, zeigen, dass die Raten
derjenigen Frauen, die sich nach Ersttrimester-Screening und NIPT und nachfolgender Bestätigung der Diagnose durch invasive Diagnostik des DS einem Schwangerschafts-Abbruch unterziehen, z. T. deutlich sinken. Abbruchraten betragen teilweise zwischen 35 % und ca. 60 %. Der Anteil der Schwangerschaftsabbrüche nach PD des DS ist in den USA z. B. von 92 % in den Jahren 1980 – 1998 auf 67 % in den Jahren 1995 – 2011 bei anhaltend abnehmender Tendenz gesunken, obwohl zu diesem Zeitpunkt NIPTs praktisch noch keine Rolle spielten [4].
In der Vergangenheit haben Frauen vor allem wegen des eingriffsbedingen Fehlgeburtenrisikos eine invasive PD meist nur dann durchführen lassen, wenn im Falle eines positiven Befundes ein Schwangerschaftsabbruch für sie auch eine ernsthafte Option darstellte. Diese Auffassung hat sich vor dem Hintergrund der Verfügbarkeit nichtinvasiver Methoden offensichtlich teilweise verändert. Mit dem Wegfall des eingriffsbedingten kindlichen Risikos entfällt das zentrale Argument in dieser Begründung.
Zunehmend nehmen vor allem junge Frauen, für die ein Abbruch nicht in Frage kommt, den risikolosen NIPT auch deshalb in Anspruch, um sich auf die Geburt eines Kindes mit DS einstellen zu können.
Schwangerschaftsabbrüche nach NIPT erfolgen deutlich früher. So lag in einer Studie der Columbia University der Anteil der Abbrüche vor der 14. SSW im Jahre 2014 bei mehr als 30 %, während dieser Anteil vorher meist unter 15 % lag [5].
Auswirkungen von PD auf die Zahl der Geburten von Kindern mit Down-Syndrom
Obwohl ein höherer Anteil von Schwangerschaften mit DS zunehmend auch bei jüngeren Frauen pränatal diagnostiziert wird und in der Folge auch vermehrt Schwangerschaftsabbrüche erfolgen, ist schwer abschätzbar, welche Folgen NIPTs auf die Anzahl von Kindern mit DS haben wird. Untersuchungen, z. B. aus den USA, England und Wales und den Niederlanden, zeigen, dass die Zahl der geborenen Kinder mit DS bisher dort nur sehr geringfügig abgenommen hat. Hauptgrund hierfür ist, dass aufgrund des steigenden Alters der Schwangeren ein deutlicher Anstieg der Zahl der Kinder mit DS zu erwarten wäre. In England und Wales wurde aus diesem Grund zwischen 1989/1990 und 2007/2008 von einer Zunahme von 71 % ausgegangen. Die tatsächliche Zahl der geborenen Kinder mit DS hat sich aufgrund beider Effekte lediglich um 1 % verringert. Bemerkenswert zu beobachten ist, dass gleichzeitig der Anteil pränatal diagnostizierten DS bei Frauen, die jünger als 37 Jahre waren, von 3 % (1989 – 1990) auf 43 % (2007 – 2008) gestiegen ist [6].
Eine Vorhersage der zukünftigen Inanspruchnahme pränataler Untersuchungen zur Erkennung kindlicher Chromosomenstörungen ist nicht sicher möglich. Die gelegentlich geäußerte Vermutung, es würden bald keine Kinder mit DS mehr geboren werden, wird jedoch sicher nicht zutreffen. Dies würde voraussetzen, dass alle Schwangeren diese Untersuchung in Anspruch nehmen werden und im Falle der Bestätigung des Befundes DS auch einen Schwangerschaftsabbruch vornehmen ließen. Bedacht werden sollte weiterhin, dass aufgrund vieler Faktoren die durchschnittliche Lebenserwartung von Menschen mit DS, z. B. in den USA 1960 noch weniger als 10 Jahre betrug und bis zum Jahr 2000 schon auf mehr als 50 Jahre angestiegen war, wodurch die Prävalenz zugenommen hat [7].
Ausschließen lässt sich jedoch keinesfalls, dass die Abbruchraten längerfristig zunehmen könnten.
NIPT als Regelleistung der Schwangerenvorsorge durch die GKV?
Seit vielen Jahren ist eine Kostenübernahme invasiver PD zur vorgeburtlichen Diagnose von Chromosomenstörungen bei Frauen, die 35 Jahre und älter sind, durch die Solidargemeinschaft der Versicherten möglich und offensichtlich gesellschaftlich akzeptiert.
Nachfolgend sollen Möglichkeiten einer zukünftigen Regelung betrachtet werden:
- Eine Nichtübernahme der Kosten von NIPT durch die GKV wird aus ethischen Gründen mit unterschiedlichen Argumenten, z. B. einer "Routinisierung", wachsendem Druck auf Schwangere zur Inanspruchnahme von NIPT u. a. m. vertreten. Nicht mehr begründbar wäre bei dieser Option dann jedoch die weiterhin mögliche Kostenübernahme für die wesentlich risikoreichere invasive Diagnostik von Frauen, die 35 Jahre und älter sind. Oder ist bei dieser Option für eine Frau über 35 Jahren eine PD mit der möglichen Konsequenz eines nachfolgenden Schwangerschaftsabbruches nach Diagnose DS ethisch eher vertretbar als bei einer 20-jährigen Schwangeren? Es ist bereits jetzt absehbar, dass ein wachsender ungeordneter Markt für Ersttrimester-Screening und NIPT und damit eine zunehmende Versorgungsungleichheit entstehen wird.
- Eine Begrenzung der Übernahme der Kosten durch die GKV auf Frauen mit erhöhten Risiken klingt scheinbar logisch und wird z. B. vom Nationalen Ethikrat, vertreten. Diese Option hat den entscheidenden Nachteil, dass hierbei definiert werden muss, wann ein "erhöhtes Risiko" überhaupt vorliegt und vor allem, wie es ermittelt werden soll. Sind damit etwa Frauen mit "erhöhtem" Alter oder auffälligem Ersttrimester-Screening gemeint? Es macht keinen Sinn, den Zugang zu NIPT von dem im Vergleich hierzu gänzlich unzulänglichen Ersttrimester-Screening (PPW: 66 % vs. 5 %!) abhängig zu machen. Eine Begrenzung der Kostenübernahme auf Frauen, die z. B. 35 Jahre und älter sind, hätte lediglich eine mengenmäßige Begrenzung zur Folge und wäre allenfalls unter groben Kostengesichtspunkten zu diskutieren, da die Zahl der Folgeuntersuchungen schwer abschätzbar sein wird.
- Die Übernahme der Kosten für NIPT durch die GKV für alle Schwangeren ist unter der Annahme sinnvoll, dass die bisherige Praxis einer GKV-Finanzierung invasiver PD für Frauen, die 35 Jahre und älter sind, nicht mehr wirklich begründbar ist, wenn ein sehr sensibles Screening-Instrument existiert, das für Ausschlüsse des Down-Syndroms praktisch diagnostischen Charakter besitzt. Der Wunsch Schwangerer, möglichst früh in Erfahrung zu bringen, ob ihr Kind eine Chromosomenstörung haben wird, wird nicht begrenzt werden können. NIPT wird weltweit zunehmend in Anspruch genommen und führt im Vergleich zu anderen vorgeburtlichen Untersuchungsstrategien zu einer drastischen Reduktion invasiver diagnostischer Eingriffe und damit untersuchungsbedingter Fehlgeburten (Tab. 1).
Forderung nach umfassender Aufklärung und Beratung aller Schwangeren ist zwingende Voraussetzung und große Herausforderung
Die Deutsche Gesellschaft für Humangenetik (GfH) hat in ihrer "Stellungnahme zur Analyse fetaler DNA aus dem mütterlichen Blut" bereits im Jahr 2012 betont, dass NIPT "als eine Weiterentwicklung nichtinvasiver Testverfahren zu einer risikolosen, in der frühen Schwangerschaft einsetzbaren Untersuchungsmethode prinzipiell positiv zu bewerten ist und wegen des Wegfalls des eingriffsbedingten Risikos keiner Schwangeren vorenthalten werden kann, bzw. allen Schwangeren verfügbar gemacht werden sollte" [8]. Diese Forderung darf jedoch keinesfalls als eine an jede Schwangere gerichtete Aufforderung missverstanden werden, diese Verfahren in Anspruch zu nehmen.
Es muss die individuelle informierte Entscheidung jeder einzelnen Schwangeren bzw. jedes einzelnen Paares sein, ob sie einen nichtinvasiven Pränataltest in Anspruch nehmen möchten. Eine zentrale Voraussetzung hierfür ist die Sicherstellung einer kompetenten umfassenden Beratung, die derzeit nicht gegeben ist.
Die GfH hat in ihren Verlautbarungen keine Aussage zur Finanzierung des NIPT getroffen. Sie "verkennt nicht, dass durch die Entwicklung derartiger Untersuchungsverfahren die gesellschaftliche Bewertung von erkennbaren Behinderungen/Entwicklungsstörungen beeinflusst wird ..." und fordert eine umfassende qualifizierte Beratung [8]. Diese muss die gesamte Problematik vorgeburtlicher Screening- und Diagnoseverfahren umfassen, die nicht marktgesteuert sein darf. Hierzu zählt auch die Information zu den realistischen Folgen der Chromosomenveränderung für betroffene Menschen und deren Familien selbst. Dies ist in einer Gesellschaft mit 97.271 Schwangerschaftsabbrüchen (2017) nach der Beratungsregel und 3.911 aus medizinischer Indikation (3,9 %) eine große gesamtgesellschaftliche Herausforderung. Eltern lieben ihre behinderten Kinder, für das DS ist das gut untersucht. Unabhängig davon wäre es gänzlich verfehlt, die vielfältigen und weit verbreiteten Sorgen und Ängste betroffener Familien nicht ernst zu nehmen, wie die Sorge, dass ein weiteres Kind betroffen sein könnte, die Unsicherheit über die Zukunft ihres Kindes, wenn sich die Eltern nicht mehr kümmern können, die Ängste der Mütter, dass ihre Tochter mit DS schwanger werden könnte. Diese Liste ließe sich beliebig verlängern.
In der öffentlichen Diskussion wird diese Seite jedoch nur selten angesprochen. In Anbetracht der zunehmenden Zahl genetischer Tests ist eine Begrenzung, z. B. der Kassenarztsitze für Fachärzte für Humangenetik, mit allen Folgewirkungen nicht begründbar und bedarf dringend einer Revision. Da Familien sich zunehmend auch über neue Medien informieren, sollten entsprechende Tools zur sachlichen Information unter breiter Beteiligung vieler involvierter Gruppierungen initiiert werden.
- Wir können den Zugang zu genetischen Informationen nicht verhindern.
- Wir müssen uns (vielmehr) für den verantwortungsvollen Umgang damit einsetzen.
- Unsere Bevölkerung weiß zu wenig über Erbkrankheiten und Behinderungen und deren Entstehung.
- Wir müssen das Wissen hierüber und die „neutrale“ Beratungskompetenz verbessern.
- Wir müssen uns als Gesellschaft immer wieder fragen lassen, ob wir Familien mit dem Schicksal einer Erbkrankheit diejenige Hilfe bieten, die ihnen ein würdevolles Leben ermöglicht.
Den Contra-Artikel finden Sie hier.
Interessenkonflikt: Der Autor hat bisher in keinem Fall die Durchführung eines NIPT veranlasst bzw. einen Test veräußert. Es bestehen keinerlei wirtschaftliche oder sonstige Verbindungen zu Anbietern entsprechender Tests.
Erschienen in: Kinderärztliche Praxis, 2019; 90 (2) Seite 118-133