Bewegungsstörungen im Säuglings- und Kleinkindalter sind ein häufiger Vorstellungsgrund bei der Kinderärztin oder beim Kinderarzt. Dabei kann es sich sowohl um harmlose, selbstlimitierende Störungen handeln, die keiner Therapie bedürfen, als auch um schwerwiegende Erkrankungen, die eine umfassende Diagnostik und rasche Therapieeinleitung erfordern [1, 2]. Wie kann man die Symptome richtig einordnen?
Ziel dieses Übersichtsartikels ist nicht, die Ursachen und die Pathophysiologie von Bewegungsstörungen umfassend zu erörtern. Vielmehr sollen die klinischen Charakteristika dargestellt werden, die es der Kinderärztin bzw. dem Kinderarzt vielfach erlauben, diese per Blick- oder Videodiagnose korrekt zu benennen. Zudem soll auf einige Erkrankungen mit potentieller Behandlungsrelevanz etwas detaillierter eingegangen werden.
Aus didaktischen Gründen werden im Folgenden permanente und paroxysmale Bewegungsstörungen unterschieden.
Permanente Bewegungsstörungen
Hierzu können spastische, ataktische und dyston-athetotische Formen gezählt werden. Diese lassen sich oft bestimmten Bereichen des Gehirns zuordnen.
Spastik
Ursache der Spastik ist eine Läsion der Pyramidenbahn, deren Fasern ihren Ursprung im motorischen Kortex (Gyrus präcentralis) haben, im Bereich der inneren Kapsel (Capsula interna) gebündelt werden, in Höhe der Medulla oblangata zur Gegenseite kreuzen und dann im Rückenmark zu den Armen und Beinen ziehen. Typische Symptome sind erhöhter Muskeltonus der Extremitäten mit Klappmesserphänomen, gesteigerte Muskeleigenreflexe mit verbreiterten Reflexzonen, Kloni sowie ein positives Babinski-Zeichen (Abb. 1). Häufigste Ursache ist eine frühkindliche Hirnschädigung im Rahmen einer Frühgeburtlichkeit oder perinatalen Asphyxie. Meist ist dann auch die Perinatalanamnese auffällig.
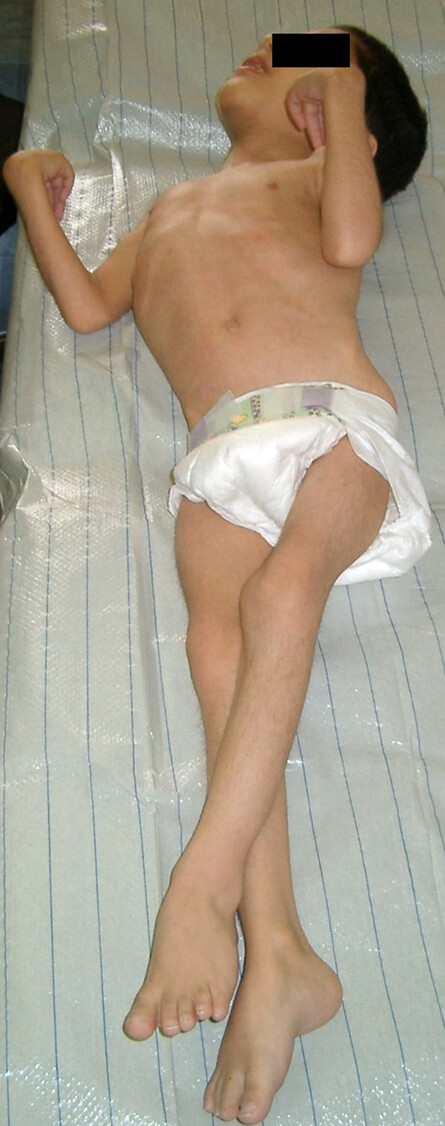
Abb. 1: 5-jähriger Junge mit schwerster spastischer Tetraparese. Beachten Sie die Streckstellung und das Überkreuzen der Beine, die Beugehaltung der Arme und Hände bei Kopfreklination und ein postives Babinski-Zeichen bereits in Ruhe
Unter einer infantilen Zerebralparese (ICP) versteht man eine Bewegungsstörung, häufig in Form einer Spastik, die entweder intrauterin oder kurz nach Geburt eingetreten ist, die nicht progredient ist, und häufig mit anderen Komorbiditäten, z. B. Intelligenzminderung oder Epilepsie, assoziiert ist. Während die ICP früher meist auf einen Sauerstoffmangel bei Geburt zurückzuführen war, dominieren heutzutage Komplikationen bei Frühgeburtlichkeit wie Hirnblutung oder periventrikuläre Leukomalazie (Abb. 2 A + B).
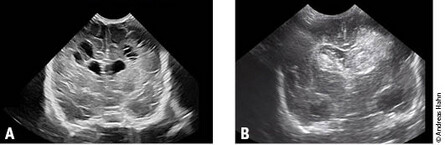
Abb.2 A + B: Schädelsonographisch ausgeprägte bilaterale periventrikuläre polyzystische Veränderungen im Rahmen einer Leukomalazie bei einem Frühgeborenen der 24. Schwangerschaftswoche (A). Bilaterale, linksbetonte Hirnblutung bei einem Frühgeborenen der 26. Schwangerschaftswoche (B).
Beides führt zur Schädigung der periventrikulären weißen Substanz. Da die Bahnen zu den Beinen näher am Ventrikel liegen als die zu den Armen, sind so verursachte ICP in aller Regel beinbetont. Finden sich eine Monoparese eines Arms oder armbetonte Paresen, ist an andere Schädigungen, z. B. einen konnatalen Mediainfarkt oder Hirnfehlbildungen, zu denken. Bei bereits intrauterin aufgetretenen Blutungen muss differenzialdiagnostisch an Mutationen in Kollagen-IV-Genen (COL4A1 o. COL4A2) gedacht werden (Abb. 3 A). Bei älteren Kindern mit ICP und nicht eindeutig auffälliger Perinatalanamnese können Erweiterungen und/oder Unregelmäßigkeiten der Ventrikelwände sowie Blutungsreste bei Verwendung sog. Häm-sensitiver Sequenzen in der Magnetresonanztomographie auf stattgehabte Blutungen hinweisen und so den V. a. eine frühkindliche Hirnschädigung erhärten (Abb. 3 B).
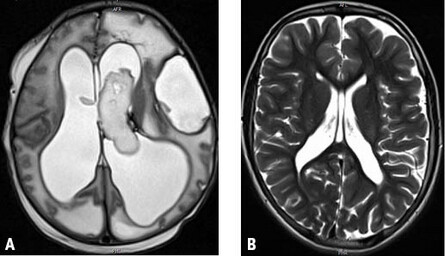
Abb. 3 A + B: Kernspintomographisch deutliche Aufweitung der Seitenventrikel mit bereits intrauterin aufgetretener intraventrikulärer Blutung links und zusätzlichem Hämatom linkshemispheral bei einem Neugeborenen mit COL4A1-Defekt (A). Unregelmäßige Begrenzung und posteriore Erweiterung der Seitenventrikel bei einem 12-jährigen Mädchen mit spastischer Diparese sowie Z. n. Frühgeburt in der 31. SSW ohne eindeutig auffällige Perinatalanamnese (B).
Ataxie
Eine Ataxie kann durch Schädigungen des Kleinhirns oder sensibler Bahnen im Rückenmark verursacht werden. Typisch sind Dysmetrie beim Greifen von Spielzeug, Intentionstremor, skandierende Sprache und breitbasiger unsicherer Gang. Liegt der Ataxie eine Rückenmarksschädigung zugrunde, steht oft die Gangataxie im Vordergrund und die Symptomatik verstärkt sich bei Augenschluss. Früh manifestierende Ataxien treten häufig mit einer Spastik im Rahmen einer ICP auf. Bei Ataxien ohne ICP handelt es sich meist um genetisch bedingte Erkrankungen [2]. Daher ist eine frühzeitige umfassende genetische Abklärung (Next-Generation-Sequencing) sinnvoll. Differenzialdiagnostisch sollte insbesondere an ein Angelman-Syndrom oder ein CDG-Syndrom gedacht werden (Abb. 4). Therapeutisch wichtig ist das Opsoklonus-Myoklonus-Syndrom (Kinsbournesche Enzephalopathie). Charakteristisch sind irreguläre Augenbewegungen und eine ausgeprägte Ataxie. Das Opsoklonus-Myoklonus-Syndrom kann entweder paraneoplastisch bei Neuroblastom oder autoimmunologisch durch Antikörper gegen Kleinhirnstrukturen bedingt sein. Eine möglichst rasche Therapieeinleitung (komplette Tumorresektion und/oder immunsuppressive Behandlung) beeinflusst die Prognose positiv [3].
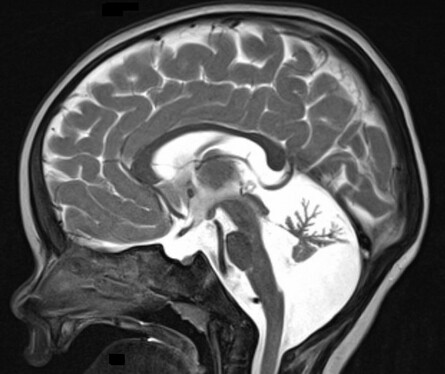
Abb. 4: Sagittales Kernspintomographiebild mit ausgeprägter Kleinhirnatrophie bei einem einjährigen Jungen mit CDG-Syndrom 1 a und Ataxie.
Dystonie
Dystone Bewegungsstörungen lassen sich meist auf Schädigungen der Basalganglien zurückführen. Athetose, Tremor, Ballismus und Chorea können als Unterformen der Dystonie interpretiert werden. Oft wird in Abgrenzung zur Spastik der Begriff extrapyramidale Bewegungsstörungen gebraucht. Klinisch finden sich unwillkürliche, oft schmerzhafte, Verkrampfungen von Muskelgruppen, die zu ungewöhnlichen Körperhaltungen und unkontrollierbaren Bewegungen führen. Die Dystonie kann einzelne Muskelgruppen (fokal, segmental) oder alle Muskeln (generalisiert) betreffen [2]. Ähnlich wie die Ataxie treten dystone Bewegungsmuster bei Kindern häufig in Kombination mit einer Spastik bei perinataler Hirnschädigung auf (spastisch-dystone ICP).
Eine bei in Deutschland geborenen Kindern sehr selten auftretende Hirnschädigung ist der Kernikterus im Rahmen einer schweren Hyperbilirubinämie (Abb. 5 A). Aufgrund der Migration aus Ländern mit weniger gut entwickelter Perinatalversorgung muss an dieses Krankheitsbild aber wieder vermehrt gedacht werden. Charakteristisch ist die Kombination aus schwerer Dystonie, Schwerhörigkeit oder Taubheit und vertikaler Blickparese. Gefürchtet sind zudem Stoffwechselentgleisungen bei metabolischen Erkrankungen, wie z. B. der Glutarazidurie Typ 1 oder Harnstoffzyklusdefekten, die zu irreversiblen Basalganglienschädigungen mit therapieschwieriger Dystonie führen können (Abb. 5 B).
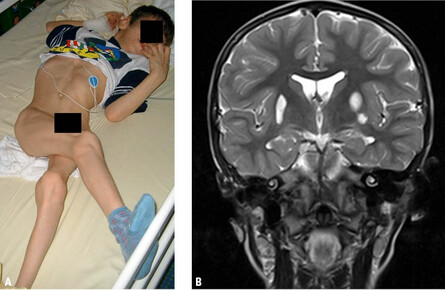
Abb. 5 A+B: Siebenjähriger Junge mit schwerer dystoner Bewegungsstörung, Taubheit und vertikaler Blickparese bei Z. n. Kernikterus (A). Koronares MRT-Bild eines sechsjährigen Jungen mit Basalgangliennekrosen aufgrund einer Mutation im NDUFV1-Gen (sog. infantile bilaterale striatale Nekrose = IBSN) (B).
Differenzialdiagnostisch wichtig ist die Segawa-Dystonie. Ursache dieser autosomal-dominant vererbten Neurotransmitterstörung sind Defekte im GCH1-Gen. Da betroffene Patientinnen und Patienten oft sehr eindrücklich auf eine L-Dopa-Therapie ansprechen, sollte bei jeder Patientin und jedem Patienten mit ungeklärter Dystonie oder auch Spastik eine probatorische Behandlung erwogen werden.
Paroxysmale Bewegungsstörungen
Bei vielen paroxysmal auftretenden Bewegungsstörungen kommen epileptische Anfälle als Differenzialdiagnose in Frage. Die Unterscheidung zwischen einem epileptischen Anfall und nichtepileptischen Phänomenen ist auch für Geübte oft nicht einfach. Die Durchführung eines Elektroenzephalogramms, wenn möglich mit Aufzeichnung eines Ereignisses, ist sehr hilfreich. Kann während eines paroxysmalen Geschehens kein Anfallsmuster registriert werden, ist ein epileptischer Anfall mit hoher Wahrscheinlichkeit ausgeschlossen [1, 4, 5].
Einen Überblick über paroxysmale Bewegungsstörungen im Säuglings- und Kleinkindalter gibt Tabelle 1.
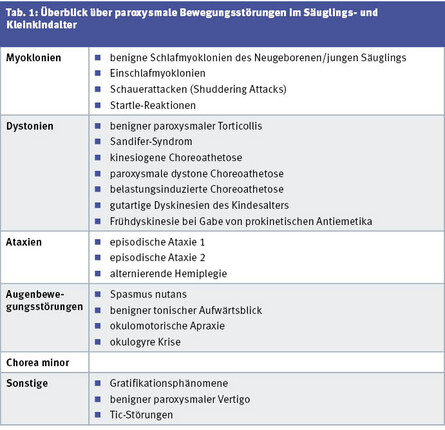
Myoklonien
Unter Myoklonien versteht man kurze unwillkürliche Zuckungen einzelner Muskeln oder Muskelgruppen.
Benigne Schlafmyoklonien des Neugeborenen: Gutartige Schlafmyoklonien des Neugeborenen sind eine wichtige Differenzialdiagnose zu Neugeborenenkrampfanfällen. Typisch sind irreguläre oder rhythmische Myoklonien und Kloni der Extremitäten im Schlaf. Die oft clusterhaft auftretenden Myoklonien erfassen nicht das Gesicht und auch der Rumpf ist meist nur leicht betroffen. Die Symptomatik kann sehr heftig ausgeprägt sein. Die Myoklonien verschwinden durch Wecken immer sofort, das EEG ist unauffällig und die Symptomatik endet spontan innerhalb der ersten 6 Lebensmonate. Phenobarbital und Benzodiazepine können die Myoklonien verstärken und Anlass zu unnötiger Diagnostik und Therapie geben [4].
Einschlafmyoklonien: Einschlafmyoklonien können sehr heftig sein und sogar zum Erwachen der Kinder führen, sollten aber differenzialdiagnostisch selten ein Problem darstellen.
Schauerattacken (Shuddering Attacks): Diese Bewegungsstörung tritt meist bei Säuglingen zwischen dem 3. und 8. Lebensmonat auf. Extremitäten, Rumpf und geringer ausgeprägt auch der Nacken zeigen kurze tremorartige Zuckungen mit einer Frequenz von circa 10 Hz, die sehr diskret ausgeprägt sein können. Das Bewusstsein der Kinder ist unbeeinträchtigt [4, 6].
Startle-Reaktionen: Unter Startle- oder Schreckreaktionen versteht man heftige, unwillkürliche Reaktionen auf einen plötzlich auftretenden Reiz, die mehr oder weniger große Teile der Körpermuskulatur umfassen und sich in einem Zusammenzucken des Körpers oder von Körperteilen äußeren. Meist werden sie durch akustische Reize ausgelöst [7].
Eine wichtige Differenzialdiagnose von Startle-Anfällen ist die Hyperekplexie. Das Krankheitsbild wird durch Defekte eines im Rückenmark exprimierten Glyzinrezeptors ausgelöst. Die Erkrankung kann sich in der Neugeborenenperiode mit tonischer Versteifung des gesamten Körpers und schwerer Zyanose manifestieren. Die zunehmende Schreckhaftigkeit bei plötzlichen lauten Geräuschen wird oft erst in den kommenden Wochen und Monaten deutlich. Die Erkrankung spricht gut auf Benzodiazepine (z. B. Clonazepam) an [7]. Ausgeprägte Startle-Reaktionen finden sich gelegentlich bei neurometabolischen Erkrankungen; insbesondere bei der GM2-Gangliosidose.
Dystone Bewegungsstörungen
Benigner paroxysmaler Torticollis: Der benigne paroxysmale Torticollis dauert meist mehrere Stunden (manchmal Tage) an und wird üblicherweise von Übelkeit und Erbrechen begleitet. Der Kopf bleibt dauerhaft gewendet. Manchmal beugt sich auch der Rumpf in die gleiche Richtung. Selten tritt der paroxysmale Torticollis infektassoziiert auf. Differenzialdiagnostisch ist an Tumore der hinteren Schädelgrube zu denken [2].
Sandifer-Syndrom: Das Sandifer-Syndrom bezeichnet tonische Kopfwendungen, die auch Extremitäten und Körper einbeziehen können. Die Kinder nehmen dabei z. T. bizarre Haltungen ein. Ursprünglich wurde angenommen, dass dieses Syndrom nur bei Kindern mit ICP oder syndromalen Erkrankungen und gastroösophagealem Reflux oder axialer Gleithernie auftritt. Es können aber auch Kinder ohne ICP betroffen sein [8].
Choreoathetosen: Bei der kinesiogenen Choreoathetose kommt es durch schnelle oder wiederholte Bewegungen (z. B.
schnelles Auf-der-Stelle-Treten) zu wilden Bewegungsstürmen, die am ehesten als hampelmannartig zu beschreiben sind. Die Zustände sind meist kürzer als eine Minute. Carbamazepin und Benzodiazepine wirken oft bereits in niedriger Dosis. Viele Fälle treten familiär auf. Die Erkrankung ist genetisch heterogen [2, 4].
Die paroxysmale dystone Choreoathetose lässt sich durch Stress, Tee, Koffein, Cola etc. auslösen. Die Attacken dauern mehrere Minuten und können sich oft hintereinander wiederholen. Es kommt zu heftigen ausfahrenden ballistischen und dystonen Bewegungen, oft mit Sturz. Eine Therapie mit Antiepileptika kann versucht werden. Mutationen im Myofibrillogenesis-Regulator-1-Gen sind ursächlich [2, 4].
Bei der belastungsinduzierten Choreoathetose kommt es nach körperlicher oder psychischer Belastung zu Dyskinesien. Differenzialdiagnostisch muss an mildere Formen eines Glukosetransporterdefektes (GLUT1) gedacht werden. In diesen Fällen kann eine ketogene Diät die Symptomatik beheben. Schwerere Formen des GLUT1-Mangels manifestieren sich im Säuglings- oder frühen Kleinkindalter und gehen mit globaler Entwicklungsverzögerung, Krampfanfällen und einer nicht einfach zu klassifizierenden Bewegungsstörung mit dystoner und ataktischer Komponente einher [2, 4].
Harmlose, nicht behandlungswürdige und selbstlimitierende Bewegungsstörungen sind sog. gutartige Dyskinesien des Kindesalters. Hierbei handelt es sich um komplexe Bewegungsabläufe bei freudiger Erregung oder Anspannung [4].
Frühdyskinesien können auch schon bei Kleinkindern durch Gabe von eigentlich nicht indizierten prokinetischen Antiemetika wie Metoclopramid oder Domperidon beobachtet werden. Die Symptomatik sistiert rasch nach Gabe von Biperiden [9].
Ataktische Bewegungsstörungen
Die episodische Ataxie Typ 1 ist charakterisiert durch Episoden mit zerebellärer Ataxie, die Sekunden bis wenige Minuten anhalten. Zusätzlich zeigen Betroffene zwischen den Attacken Myokymien, d. h. langsame wellenförmige Muskelkontraktionen, die an der Hautoberfläche sichtbar sind. Die Erkrankung wird durch Defekte des spannungsabhängigen Kaliumionenkanals KCNA1 ausgelöst. Fälle mit isolierter Myokymie, aber auch nur mit Ataxie und mit Epilepsie kommen vor. Bei der episodischen Ataxie Typ 2 dauern die Ataxieepisoden meist 10 bis 20 Minuten. Zusätzlich finden sich oft interiktal ein Nystagmus oder Augenbewegungsstörungen. Ursächlich sind Defekte im CACNA1A-Gen. Beide o. g. Formen sprechen gut auf Acetazolamid an [2, 4].
Die alternierende Hemiplegie des Kindesalters ist ein progredient verlaufendes Krankheitsbild, das zu Beginn der Erkrankung mit einer Epilepsie verwechselt werden kann. Zudem treten im Verlauf bei einem Teil der Patientinnen und Patienten epileptische Anfälle auf. Die Erkrankung beginnt bereits im ersten Lebensjahr mit schlaffen, wechselnd lateralisierten Hemiparesen, tonischen Versteifungen, Nystagmus und autonomen Phänomenen (Blässe etc.). Die Attacken kommen oft mehrfach monatlich vor. Manchmal wechselt die Hemiplegie im Anfall die Seite noch bevor die zuerst betroffene Körperhälfte sich wieder erholt hat. Im Schlaf verschwindet die Symptomatik. Besserung kann mit dem Kalziumantagonisten Flunarizin und evtl. auch mit Nemantin, Chloralhydrat oder Niaprazin erzielt werden. In mehreren Fällen konnten Defekte im ATP1A2-Gen identifiziert werden [1, 2, 4, 5].
Augenbewegungsstörungen
Spasmus nutans: Der Spasmus nutans besteht aus einem asymmetrischen Nystagmus, einer Kopfschiefhaltung und Kopfnicken. Die Symptomatik kann dauerhaft oder auch episodisch auftreten und ist meist selbstlimitierend. In mehreren gut dokumentierten Fällen stellten sich jedoch verschiedene ZNS- oder Retinaläsionen als ursächlich heraus. Eine ausführliche Diagnostik ist daher sinnvoll [10].
Paroxysmaler tonischer Aufwärtsblick: Der paroxysmale tonische Aufwärtsblick tritt in der Regel im 1. oder 2. Lebensjahr auf. Es kommt zu tonischen Augenbewegungen nach oben, die meist weniger als eine Minute dauern. Die Episoden können sich mehrfach am Tag wiederholen. Beim Versuch nach unten zu blicken, kommt es zum Nystagmus. Die Symptomatik sistiert meist spontan. Analog zum Aufwärtsblick wurde vereinzelt auch ein tonischer Abwärtsblick beschrieben [11].
Okulomotorische Apraxie: Diese Augenbewegungsstörung wird nicht selten mit myoklonischen Anfällen verwechselt. Die Kinder können die Bulbi nicht zielgerichtet bewegen. Um eine Blickrichtungsänderung zu erzielen, führen sie ruckartige Bewegungen des gesamten Kopfes aus. Viele der beschriebenen Patientinnen und Patienten zeigten auch eine mehr oder minder stark ausgeprägte Entwicklungsverzögerung. Die okuläre Symptomatik bessert sich im Verlauf zumeist leicht [4].
Okulogyre Krisen: Hierunter versteht man unwillkürliche symmetrische dystone Bulbusbewegungen in eine Richtung, die Sekunden bis mehrere Minuten, selten sogar Stunden, anhalten, und mit Kopfwendung oder auch Versteifung weiterer Körperteile einhergehen können. Bei Säuglingen mit deutlicher muskulärer Hypotonie und generalisierter Entwicklungsverzögerung muss an Neurotransmitterstörungen wie den seit Kurzem mittels Gentherapie behandelbaren Aromatischen Aminosäure-Decarboxylase- (AADC)-Mangel gedacht werden [12].
Chorea minor
Unter einer Chorea minor versteht man unkontrollierbare blitzartig ausfahrende Bewegungen insbesondere der Hände und/oder der Gesichts- und Schlundmuskulatur. Oft bestehen auch eine muskuläre Hypotonie und eine Areflexie. Die Erkrankung ist zumeist autoimmunologisch bedingt. Sie kann im Anschluss an eine Streptokokkeninfektion (z. B. Scharlach), aber auch unabhängig davon auftreten. Differenzialdiagnostisch sind andere Erkrankungen mit Affektion der Basalganglien zu bedenken. Die Behandlung richtet sich nach der zugrundeliegenden Ursache.
Sonstige
Gratifikationsphänomene: Gratifikationsphänomene bzw. kindliche Masturbationen treten vorwiegend innerhalb der ersten 5 Lebensjahre bei Mädchen auf. Typisch sind gekreuzte und aneinander gepresste Beine bzw. Oberschenkel. Die Kinder wirken abwesend und blicken verklärt. Oft bemerkt man eine Gesichtsrötung. Rhythmische Beckenbewegungen sind typisch, können aber auch ganz fehlen. Manchmal pressen die Mädchen ihren Schritt auch gegen Gegenstände (Tisch- oder Stuhlbeine). Versucht man die Kinder anzusprechen, reagieren sie nur unwillig. Beendet man die Bewegung aktiv, werden sie ärgerlich und fahren anschließend wieder damit fort. Die Symptomatik kann sehr ausgeprägt sein, sich mehrfach am Tag wiederholen und sich über längere Zeiträume erstrecken. Es liegen keine psychologischen Konfliktsituationen zugrunde. Die Therapie besteht in Abwarten [13].
Benigner paroxysmaler Vertigo: Der benigne paroxysmale Vertigo betrifft Kinder in den ersten 5 Lebensjahren. Der Beginn ist plötzlich. Die Patientinnen und Patienten legen sich zu Boden oder halten sich an Gegenständen oder Personen fest. Die Attacken dauern meist ca. eine Minute. Das Bewusstsein bleibt erhalten. Oft werden die Kinder blass. Manchmal können die Eltern einen Nystagmus beobachten. Die Episoden treten meist nur wenige Male im Jahr auf, sind unangenehm aber harmlos [14].
Tic-Störungen: Unter Tics versteht man kurze nicht rhythmische Kontraktionen einzelner Muskeln oder Muskelgruppen oder Lautäußerungen, die keinem erkennbaren Zweck dienen. Unterschieden werden können motorische (z. B. Augenblinzeln oder Stirnrunzeln) und vokale (Räuspern, Schmatzen, Bellen) Tics sowie einfache und komplexe Tics (z. B. Springen, zwanghaftes Nachahmen oder Wiederholen von Bewegungsabläufen). Bestehen komplexe Tics länger als ein Jahr und gehören auch vokale Tics wie Koprolalie zur klinischen Symptomatik, ist an ein Tourette-Syndrom zu denken.
Die Diagnosestellung bei einfachen Tics ist zumeist anhand von Anamnese und Klinik unproblematisch. Symptomatik und Frequenz der Tics sind häufig fluktuierend und die Prognose ist meist günstig. Eine medikamentöse Behandlung mit Tiaprid kann bei stark ausgeprägter Symptomatik und hohem Leidensdruck des Kindes indiziert sein [15].
Fazit
Die in dieser Arbeit gegebene Übersicht über Bewegungsstörungen im Säuglings- und Kleinkindalter macht deutlich, dass viele dieser Erkrankungen bereits von der niedergelassenen Kinderärztin bzw. dem niedergelassenen Kinderarzt allein aufgrund ihrer typischen Charakteristika diagnostiziert werden können. Oft können so überflüssige Untersuchungen und unnütze Therapien vermieden werden. Oder es können Zeitpunkt und Umfang der notwendigen Diagnostik zielgerichtet geplant und die entsprechende Therapie eingeleitet werden.
- Bewegungsstörungen im Säuglings- und Kleinkindalter sind ein häufiger Vorstellungsgrund bei der Kinderärztin bzw. beim Kinderarzt.
- Die Ursachen für Bewegungsstörungen sind vielfältig und umfassen sowohl harmlose und selbstlimitierende als auch dringend abklärungs- und behandlungsbedürftige Formen.
- Eine Videoaufnahme und ein Elektroenzephalogramm sind wertvolle Hilfsmittel zur genauen Einordnung paroxysmaler Bewegungsstörungen.
- Bei Kenntnis typischer klinischer Charakteristika kann die Diagnose oft bereits durch die niedergelassene Kinderärztin/den niedergelassenen Kinderarzt gestellt werden; so können überflüssige Untersuchungen vermieden werden.
|
|
Erschienen in: Kinderärztliche Praxis, 2024; 95 (2) Seite 111-118





